近期,中国科学院合肥物质院固体所团队与合肥物质院强磁场中心、意大利帕多瓦大学、上海交通大学等研究机构合作,在铂纳米胶体球的激光辅助合成及其类酶近红外光催化治疗研究方面取得新进展,相关研究成果发表在《德国应用化学》(Angewandte Chemie International Edition)上。
金属纳米催化剂的性能受其 d 带电子结构影响显著。此前,Hammer 和 Nørskov 提出的 d 带模型指出,化学反应的活化能与吸附物与催化剂表面之间的成键和反键态密切相关,而这些特性又由催化剂的 d 带电子结构决定。铂(Pt)作为一种备受关注的金属催化剂,可通过提高其 d 带电子向吸附物成键态转移的效率,实现高效的催化过程。然而,目前直接利用近红外光激发 Pt 中的 d 带电子以产生热电子并提升催化效率仍面临诸多挑战,其核心问题在于 Pt 纳米颗粒的光吸收能力有待提高。
与金、银、铜和铝等系列等离子体金属催化剂不同,Pt难以在光照下展现出局域表面等离子体共振(LSPR)效应,并基于此激发 d 带电子形成热载流子(电子和空穴)。但Pt 的 d 带宽可延伸至费米能级,使其在费米能级附近具有较高的电子态密度,有望通过吸收低能光子激发 d 带电子到 sp 带,从而在近红外光照射下产生热电子。理论预测表明,当入射光波长处于 700 纳米至1000 纳米区间时,Pt 纳米晶体中热电子的产生效率将达到峰值。
为增强 Pt 纳米颗粒的光收集能力,研究人员设计了胶体球(Colloidosomes, Cs)结构,利用金属颗粒间的光子散射效应,提高其从可见光到近红外波段的光吸收效率。同时,将 Pt 纳米颗粒嵌入金属氧化物介电基质中,促进吸收介电表面散射的光子。研究发现,Pt 离子与Mn3O4(四氧化三锰)表面发生电化学置换反应,可形成多孔的 Pt/Mn3O4纳米复合材料,其中 Mn3O4作为牺牲剂,形成了负载超小 Pt 纳米颗粒的多孔骨架。理想情况下,这种纳米结构可转化为 Pt 金属胶体球,通过精准控制 Mn3O4的消耗量,有望形成一层紧密排列的 Pt 纳米颗粒外壳,并保留多孔结构和粗糙金属表面内部的多重光散射特性。然而,目前实验上尚未成功制备出均匀且紧密排列(颗粒间距小于1 纳米)的超小 Pt 纳米颗粒层构成的 Pt胶体球(Pt Cs)。
液相激光辐照技术能在纳米晶颗粒表面产生大量缺陷,优化界面压缩应变,构筑多晶结构,并形成富含缺陷位点的晶界。同时,晶界产生的压缩应变有助于促进Pt 离子电化学置换所需的界面氧化还原反应,这些优势有利于 Pt 元素在颗粒表面的均匀、致密分布。时域有限差分法(FDTD)分析结果表明,当Pt Cs表面颗粒间距小于1 纳米时,Pt即可获得从可见光到近红外的宽波段吸收能力;在近红外光激发下, Pt Cs 的 d 带电子将形成大量热载流子,并实现高效氧化光催化。
基于此,研究人员通过脉冲激光辐照获得富含晶界(GBs)的 Mn3O4 纳米颗粒,并将其作为理想的纳米支架,与 Pt 离子进行电偶置换反应,最终得到由尺寸为 2.2 纳米 的超小Pt颗粒组成的胶体球,颗粒间距仅为 0.3 纳米。光辅助的类酶催化测试结果表明,Pt Cs通过近红外光激发 d 带电子迅速产生热电子,并用于催化分解不同的酶底物分子,这为验证近红外光增强Pt催化过程的电子机制提供了确凿证据。与分散的超小 Pt 纳米颗粒相比,Pt 纳米胶体球表现出卓越的类过氧化氢酶(CAT)和类氧化酶(OXD)催化能力。
此外,研究人员进一步开展了小鼠体内肿瘤治疗实验,证实Pt纳米胶体球不仅发挥了显著的近红外光增强的级联催化治疗功能,成功抑制了肿瘤生长,还实现了磁共振成像监测肿瘤内部的代谢情况,充分体现了Pt Cs作为近红外增强型纳米酶用于光催化肿瘤治疗的巨大潜力。该工作拓展了液相激光制备技术在构筑高性能纳米酶材料方面的应用。
上述工作得到了国家重点研发计划、中国科学院合肥物质院院长基金、安徽省重点研发计划等项目的支持。
文章链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202509431
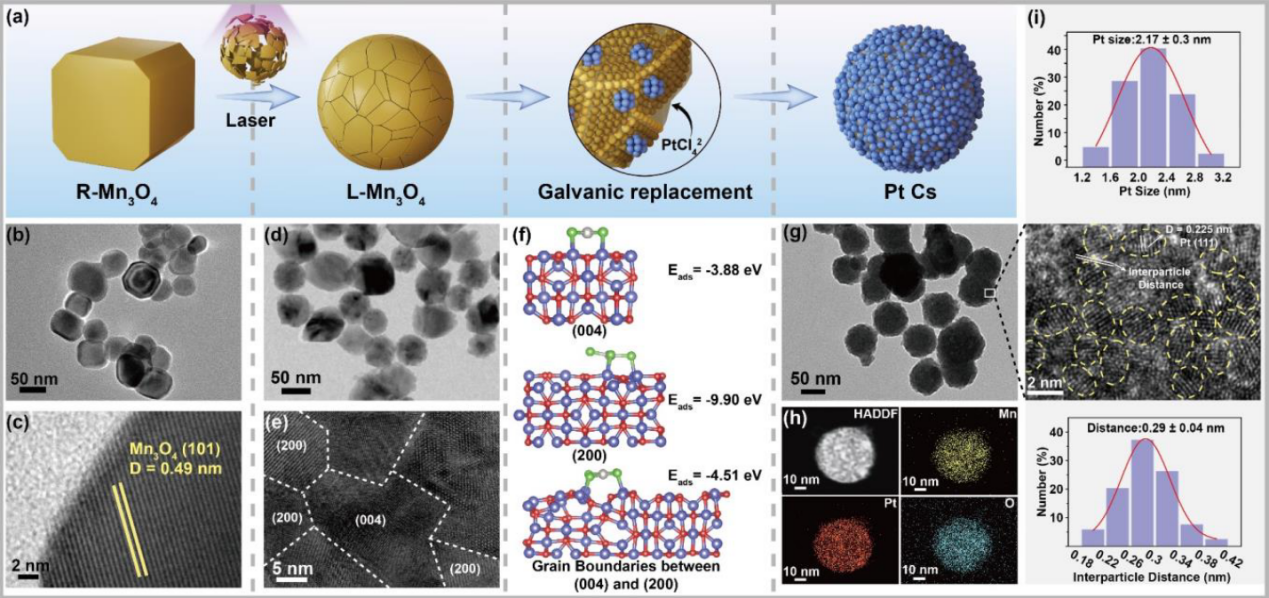
图1. Pt Cs的合成和基本表征。
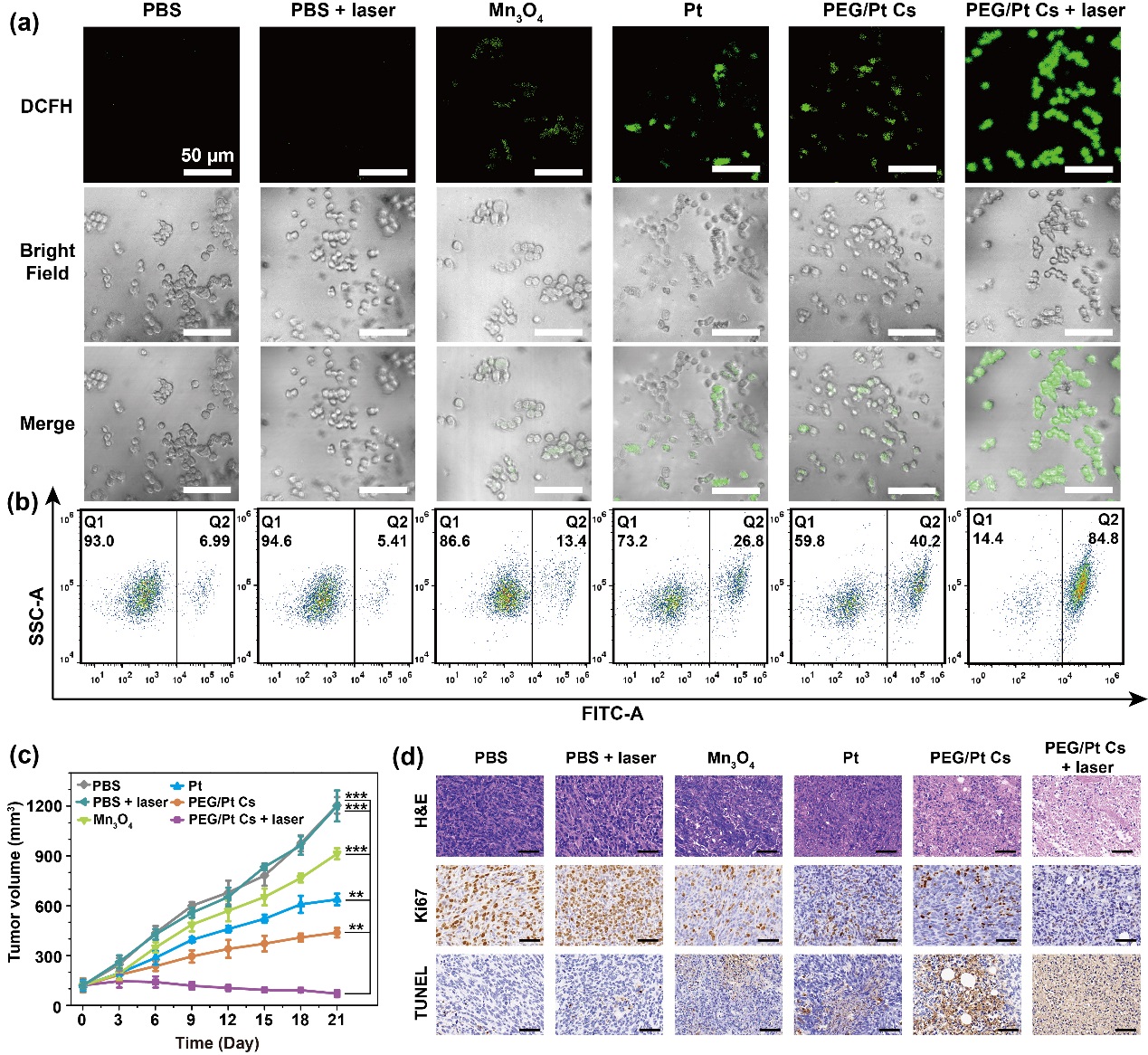
图2. Pt Cs在小鼠体内的光催化肿瘤治疗。
